9月28日,中国神经科学学会第十八届全国学术会议(CNS 2025)期间,由天桥脑科学研究院(中国)与中国神经科学学会联合主办的“BCI&AI脑机接口创新技术碧海论坛”成功举行。

今年是天桥脑科学研究院自2018年连续第8次支持CNS全国学术会议。作为由CNS评选的特色主题论坛,碧海论坛成功吸引了近400位专家学者亲临现场。钛媒体等主流科技媒体对论坛进行了直播,观看人次高达30万。
本次论坛聚焦脑机接口与人工智能的交叉领域,深度探讨了面向健康人群的脑机增强、脑机接口创新技术及类脑智能三大前沿版块。与会专家不仅分享了对脑机接口未来发展路径的前瞻思考,更提出了在人工智能辅助下的脑机接口新范式。
一、意念对话不是梦,BCI赋能健康人群实现里程碑进展

▷ 致辞/演讲嘉宾 陶虎,讲题《脑机接口-让大脑连接未来》。陶虎,脑虎科技创始人兼首席科学家。国家“万人计划”科技创新领军人才入选者、国家基金委优秀青年基金获得者、国家海外高层次人才引进计划青年项目入选者,享受国务院政府特殊津贴。中国神经科学学会脑机接口与交互分会创始主委、中国科协脑机接口产业技术路线图负责人。
天桥脑科学研究院研究员、脑虎科技(NeuroXess)创始人兼首席科学家陶虎分享了两项具有里程碑意义的最新研究成果。
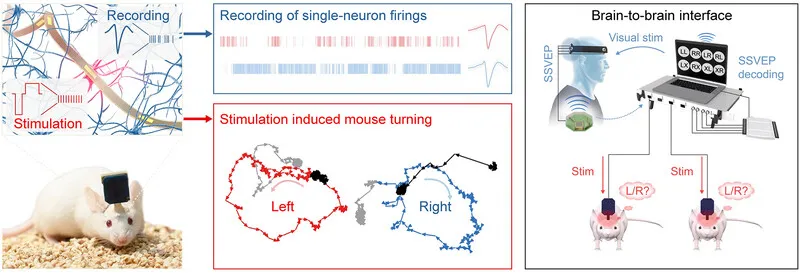
由脑虎科技自主研发的256通道超高密度柔性脑机接口系统取得了突破性进展。该系统在灵长类动物实验中实现了100%的运动意图识别准确率。在人体应用方面,经过短短一周的训练后,该系统的信息传输速率便达到了每秒4.15比特。
更引人注目的是,该技术实现了静默中文解码,超人类语速交流(突破307字/分钟,超过正常人2倍)、意念办公、双脑互联远程实时意念对话等颠覆性应用。
这些成果与国际顶尖水平相比毫不逊色。例如,马斯克的Neuralink受试者在训练一周后实现了4.60 bps的运动控制水平,而美国加州大学旧金山分校(UCSF)Edward Chang团队的解码能力为每分钟78个英语单词。脑虎科技的成果与这些国际领先水平相当甚至更优,有力地证明了中国脑机接口技术的全球领先实力。
陶虎表示,脑虎科技正致力于拓展应用场景、提升系统稳定性并降低使用成本,来加速推进相关技术的商业化应用。
二、类脑计算:定制化大模型,开启智能交互新范式

▷ 演讲嘉宾 李国齐,讲题《类脑大模型及其在脑机接口的前景》。李国齐,中国科学院自动化所研究员,脑认知与类脑智能全国重点实验室副主任,通用类脑智能大模型北京市重点实验室主任,国家杰出青年基金获得者;在Nature、Nature子刊、Science子刊等期刊和AI顶会上发表论文200余篇,论文被引用1.8万余次;主持国家自然科学基金重点项目、联合重点项目、科技部重点研发项目等30余项;担任IEEE TNNLS,IEEE TCDS和清华大学学报-自然科学版编委;曾获得中国自动化学会自然科学一等奖,ECCV最佳论文奖提名,中国算力大会最佳论文奖,曾入选北京市杰青,中国科学院百人计划,DeepTech中国智能计算科技创新人物,中国算力青年先锋人物。
中国科学院自动化所李国齐研究员认为,专门面向脑机接口优化的定制化大模型,比通用大模型更适合这一领域的发展需求。为此,他的团队开发了SpikingBrain系统,采用树突神经元作为基本计算单元,能够高效处理事件驱动和时间稀疏的脑电信号,从而在提升信号编解码性能的同时,显著降低系统功耗。
这一突破性进展,源于李国齐团队在类脑计算领域的系统性创新。他们提出的大规模脉冲神经网络计算理论,成功将脉冲神经网络(SNN)与主流人工神经网络(ANN)的性能差距从20年缩短至1年。此外,他们开发的MetaLA统一框架在性能上已超越Mamba架构。
这些前沿成果,配合低功耗类脑芯片和全栈式训练平台,为脑机接口技术开辟了新路径,展现出类脑计算与大模型融合的巨大潜力。未来,这项技术有望实现更精准的信号处理和更自然、高效的人机交互。
三、纳米智能:探索脑机交互的“微观”路径

▷ 演讲嘉宾 贺强,讲题《纳米机器人与BCI:探索人脑与机器的微观连接》。贺强,哈尔滨工业大学教授,于2003年在中国科学院化学研究所获得博士学位。他提出了胶体马达、超分子胶体马达和游动纳米机器人的概念。是首位利用可控化学组装技术构建集自推进和智能药物递送于一体的超分子胶体马达的学者。基于此,他开发了多种可注射的游动纳米机器人,并将其应用于重大疾病的精准治疗。已发表200多篇同行评议论文,并拥有24项专利。目前,他担任中国化学会胶体与界面化学专业委员会成员,以及Small,ChemNanoMat和Colloid and Surface A的编委。
传统脑机接口主要依赖植入电极,而哈尔滨工业大学贺强教授另辟蹊径:将纳米机器人集群作为一种全新的脑机交互范式。这种“自下而上”的方法,通过纳米机器人的自组织行为,实现从个体到集群、从微观到宏观的信息传递与功能调控。
作为国际上首个成功研发自推进、一体化超分子胶体的团队,贺强教授将化学动力学与纳米技术相结合,开发出一种突破性的智能纳米系统。通过可控化学组装技术,这些纳米机器人不仅能主动穿越血脑屏障,还能响应光、磁场等外部刺激实现集群协同。与传统电极植入相比,这种柔性的微观调控方式大大降低了创伤风险,为脑疾病的精准治疗和脑机交互开辟了全新途径,展现了智能纳米系统在未来医疗领域的变革性潜力。
四、聚焦超声波:实现大脑深部的无创精准调控

▷ 演讲嘉宾 Jan Kubanek,讲题《聚焦超声神经调控和脑机接口》。Jan Kubanek,生物医学工程师和神经工程师,华盛顿大学生物医学工程/神经科学博士,他曾在斯坦福大学进行博士后深造,目前是犹他大学的助理教授。他的实验室开发了一种能够对人类大脑深部回路进行精确、可控调节的设备。已发表的研究表明,该设备可调节慢性疼痛、抑郁症和特发性震颤的症状。该方法目前正用于关键的临床试验。
来自犹他大学的Jan Kubanek介绍了由其团队开创的一种突破性的超声波脑机交互技术。不同于传统侵入式电极,这项技术利用超声波能穿透颅骨的特性,通过微秒级的精确聚焦,实现了对基底节和丘脑等大脑深部结构的非侵入性调控,创新性地解决了超声波在颅骨传导时的衰减问题,确保了治疗剂量的精准递送。
临床研究显示,这项技术能有效治疗特发性震颤、重度抑郁症和慢性疼痛,并能诱导持久的神经可塑性改变。特别是在慢性疼痛治疗中,仅需40分钟的扣带回刺激就能显著改善疼痛强度。目前,这一突破性技术已进入多中心临床试验阶段。更令人振奋的是,高频超声波技术已实现单细胞级别的精确调控,预示着人类与环境、人与人之间可能出现全新的认知互动方式。
五、智能双向进化:人机共生,重塑未来

▷ 演讲嘉宾 张越一,讲题《类脑计算驱动的脑机接口》。张越一,集智进化(MiroMind)AI研究员。已发表期刊会议论文100余篇(包括CCF-A类会议文章或IEEE汇刊文章50余篇),申请/授权中国发明专利20余项。曾主持国家自然科学基金青年项目、面上项目,参与科技部科技创新 2030项目。现任中国图形图像学会多媒体专委会副秘书长,参与组织过中国多媒体大会(ChinaMM)等活动。所指导的学生中多人次获得中国科学技术大学研究生国家奖学金和专项奖学金。目前的研究方向为:脑启发多模态大模型与智能体。
MiroMind AI研究员张越一提出,要让人类智能与人工智能相互启发、共同进化。
他指出,从最初的感知机到如今丰富的人工神经网络,神经科学的发展为计算领域带来了革命性突破。通过模仿大脑架构,我们创造出了此前无法实现的计算解决方案。
更重要的是,这种影响是双向的。深度学习不仅从大脑获得灵感,反过来也帮助我们更好地理解大脑的工作机制。通过优化人工神经网络,观察其中行之有效的模式,我们得以重新审视神经连接,深入了解大脑的组织方式。这种双向互动正在开启认知科学的新篇章。
正如天桥脑科学研究院与MiroMind创始人陈天桥先生所言:
人类不仅是AI的创造者,也是其演化路径的决定者。AI与人类共同组成生态系统,互动中形成反馈循环,重塑个体认知与社会结构。未来,最终具有自我意识的人工智能,是在镜像人类智能长期记忆之后实现人类智能和人工智能的共同进化。
本次碧海论坛不仅是一场前沿技术的集中展演,更是一次对未来的深刻展望。从超高密度柔性接口到定制化大模型,从纳米机器人到无创超声波,我们正在从不同维度推动脑机接口技术的边界。这些技术突破正在加速人机共生时代的到来,共同描绘出一幅人类智能与人工智能深度融合、共同进化的宏伟蓝图。